Studie: Zeit für einen Wandel bei der Aminosäuren-Analytik (AAA)
Die quantitative Aminosäuren-Analytik (AAA) ist entscheidend für die Diagnose von Erbkrankheiten, die den Aminosäurestoffwechsel beeinträchtigen. Die häufigsten Erbkrankheiten dieser Art sind die klassische Phenylketonurie (PKU) und die Ahornsirupkrankheit (MSUD), doch es gibt auch noch viele weitere seltene Krankheiten. Die Aminosäuren-Analytik erfordert eine hohe Empfindlichkeit und Genauigkeit. Bisher galt hierbei die Ionenaustauschchromatographie (IEC) als Goldstandard. Wie die meisten Techniken weist auch die IEC einige Nachteile auf, und eine kürzlich von Carling et al durchgeführte Studie legt nahe, dass es an der Zeit ist in den klinischen Laboratorien bei der quantitativen Aminosäuren-Analytik neue Wege zu gehen.


Die Nachteile der Ionenaustauschchromatographie (IEC)
Auch wenn die IEC in der klinischen Diagnostik als Standardmethode gilt, ist ihre Funktionsweise seit über vier Jahrzehnten unverändert geblieben. Die Methode birgt jedoch genug Nachteile, die das Prüfen anderer Techniken rechtfertigen: Zu den praktischen Nachteilen der IEC gehören unter anderem eine schlechte Retention saurer Verbindungen, die Einzelpunktkalibrierung und die Notwendigkeit von Analyseprogrammen, die einige der Einschränkungen minimieren. Ein wesentliches Hindernis für klinische Labore ist jedoch vor allem die lange Analysenzeit von mehr als 120 Minuten, die die schnelle Bereitstellung klinischer Testergebnisse beeinträchtigt und die Effizienz des routinemäßigen Workflows einschränkt.
LC-MS/MS: ein neuer Ansatz für die AAA
In einer neuen Studie wurde LC-MS/MS als alternative Methode untersucht. Forscher haben dabei IEC mit verschiedenen kommerziellen LC-MS/MS-Assays in humanen Plasmaproben verglichen, einschließlich des Chromsystems-Assays MassChrom® Amino Acid Analysis im Plasma/Serum. Nicht alle LC-MS/MS-Methoden zeigten dabei die für alle Analyten erforderliche analytische Performance. Die mit dem Chromsystems-Assay durchgeführte Analyse erbrachte jedoch mit IEC vergleichbare Daten, allerdings mit einer höheren Genauigkeit und einer viel schnelleren Analysenzeit von weniger als 19 Minuten für 48 Aminosäuren. „Die Probenvorbereitung geht schnell und einfach, dauert ungefähr 20 Minuten, und erfordert angemessene Injektionsvolumen eines manuellen Assays“, so die Autoren. Die Genauigkeit wurde durch einen kombinierten Ansatz aus chromatographischer Auflösung und Selected Reaction Monitoring (SRM) erreicht. „Der underivatisierte Ansatz hat einen Einfluss auf die Empfindlichkeit der Analyten mit einem geringen Masse-zu-Ladung-Verhältnis (m/z)“, so die Autoren weiter. Der Chromsystems-Assay war der einzige in dieser Studie, der auch die isobaren Verbindungen Leucin, Isoleucin und Alloleucin trennte, wodurch die Notwendigkeit einer Bestätigungsanalytik („second line testing“) für diese Analyten entfällt.
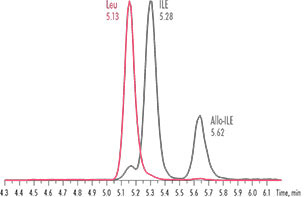

Fig.1: Der Chromsystems-Assay führt zu einer effizienten Trennung aller Isobaren wie z.B. Ile, Leu und Allo-Ile
Fazit
LC-MS/MS im Allgemeinen und der Assay MassChrom® Amino Acid Analysis im Besonderen wiesen eine analytische Performance auf, die mit der einer IEC-Analyse vergleichbar ist. Die Aminosäuren-Analytik wird jedoch viel schneller und mit höherer Genauigkeit durchgeführt. Die Verfügbarkeit eines kommerziellen CE-IVD-konformen Reagenzienkits von Chromsystems kann die für die Akkreditierung nach UKAS-Standards erforderlichen Verfahren für das Reagenzienmanagement vereinfachen. Die Autoren hielten fest: „Der Nutzen dieser Tatsache in Routineverfahren klinischer Labore sollte nicht unterschätzt werden“.
Die Studie kam schließlich zu dem Ergebnis, dass die IEC nicht mehr zwingend verwendet werden muss und auch nicht mehr als Goldstandard für die Aminosäuren-Analytik im Plasma eingestuft werden sollte, da dieselben oder bessere Ergebnisse schneller erzielt werden können. Alle Ergebnisse der Studie wurden auch im Rahmen eines Webinars dargestellt, was Ihnen on-demand zur Verfügung steht.
Letzte Aktualisierung am 20. April 2021
Dr. Rachel Carling, Scientific Director von Viapath berichtet über eine Studie die den aktuellen Goldstandard in der quantitativen Aminosäuren-Analytik (AAA), der Ionen-Austausch-Chromatographie (IEC) mit der LC-MS/MS vergleicht.


Dr. Rachel Carling, Consultant Scientist and Director of Biochemical Sciences, Viapath, UK
Rachel Carling arbeitet am Guy's und St. Thomas' Hospital, wo sie als Consultant Scientist, Director Newborn Screening und Clinical Lead, Biochemical Sciences, tätig ist. Sie ist auch Scientific Director von Viapath am GSTT-Standort. Ihr Interessengebiet sind vererbte Stoffwechselerkrankungen mit besonderem Schwerpunkt der Tandem-Massenspektrometrie.
Referenz/Originalstudie:
Carling R. S. et al, Challenging the status quo: A comparison of ion exchange chromatography with liquid chromatography–mass spectrometry and liquid chromatography–tandem mass spectrometry methods for the measurement of amino acids in human plasma, Annals of Clinical Biochemistry¸ 2020, DOI: 10.1177/0004563220933303

